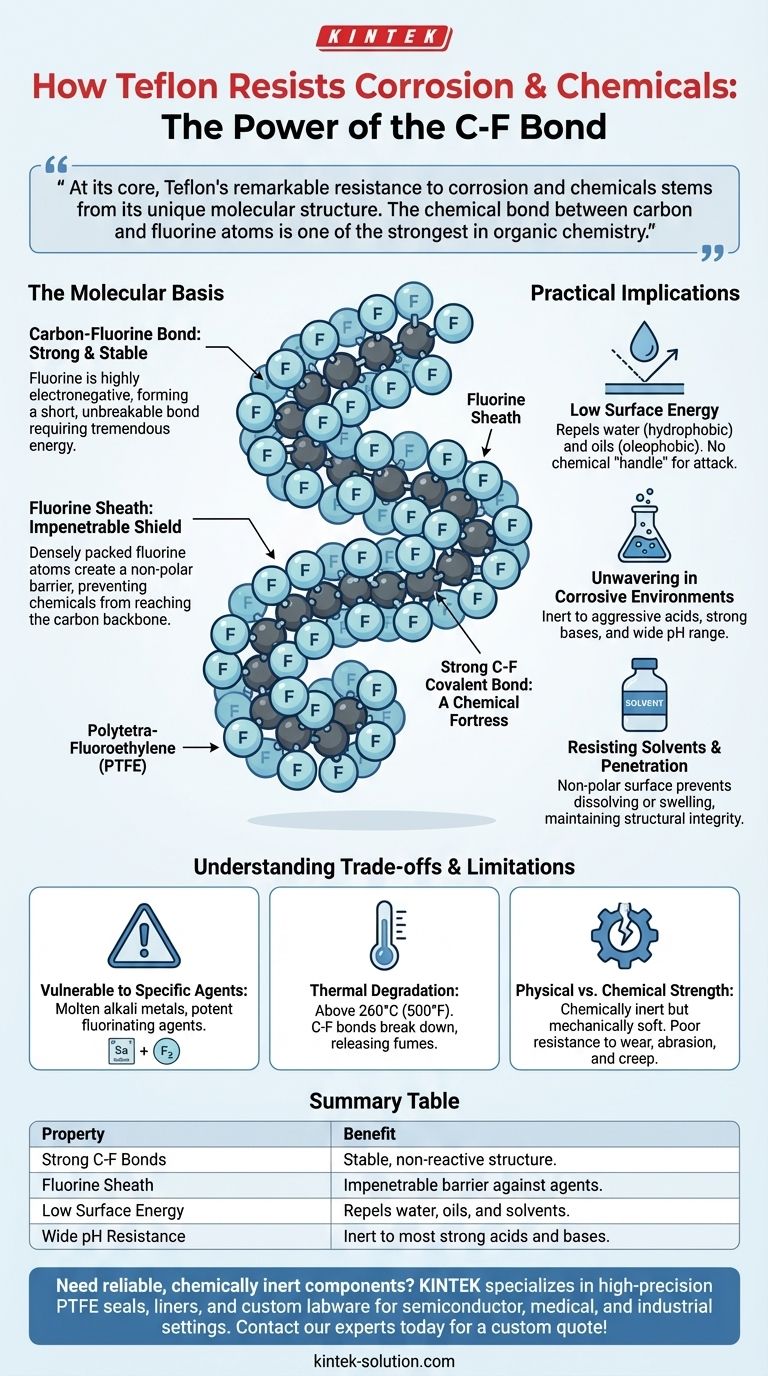
في جوهره، تنبع مقاومة التفلون المذهلة للتآكل والمواد الكيميائية من بنيته الجزيئية الفريدة. الرابطة الكيميائية بين ذرات الكربون والفلور هي واحدة من أقوى الروابط في الكيمياء العضوية. وهذا يخلق سطحًا مستقرًا وغير تفاعلي للغاية يشكل درعًا واقيًا فعالاً، مما يمنع المواد الكيميائية الأخرى من اختراق المادة أو التفاعل معها.
سر مرونة التفلون ليس مادة مضافة أو طلاء معقد؛ بل هو البساطة الأساسية لتركيبته الخاصة. تخلق ذرات الفلور غلافًا محكمًا وغير قابل للاختراق حول هيكل كربوني، مما يجعل الجزيء خاملًا كيميائيًا ومقاومًا ماديًا للهجوم.

الأساس الجزيئي لخمول التفلون
لفهم أداء التفلون حقًا، يجب أن ننظر إلى تركيبه على المستوى الذري. خصائصه ليست مصادفة؛ بل هي نتيجة مباشرة لتكوينه الكيميائي، وتحديداً بولي تترافلوروإيثيلين (PTFE).
الرابطة بين الكربون والفلور: حصن كيميائي
الرابطة بين ذرة الكربون وذرة الفلور قوية ومستقرة بشكل استثنائي. الفلور هو العنصر الأكثر سلبية كهربية، مما يعني أن لديه قوة سحب هائلة على الإلكترونات.
عندما يرتبط بالكربون، فإنه يشكل رابطة تساهمية قصيرة وقوية جدًا. تتطلب هذه الرابطة كمية هائلة من الطاقة للكسر، مما يجعل الجزيء مقاومًا للغاية للتفاعلات الكيميائية.
غلاف الفلور: درع لا يمكن اختراقه
في جزيء PTFE، تشكل ذرات الكربون الصغيرة نسبيًا سلسلة طويلة تعمل كهيكل أساسي. يتم تغليف هذا الهيكل بالكامل بذرات الفلور الأكبر حجمًا.
ينتج عن هذا "غلاف" كثيف وموحد وغير قطبي من الفلور. هذا الحاجز المادي والكهربائي يمنع المواد الكيميائية المسببة للتآكل من الوصول إلى الهيكل الكربوني الضعيف لبدء التفاعل.
طاقة السطح المنخفضة: صد جميع الغزاة
يمنح غلاف الفلور التفلون طاقة سطح منخفضة للغاية. هذا هو السبب في شهرته بأنه غير لاصق.
الخاصية نفسها تعني أنه كاره للماء (يطرد الماء) و كاره للدهون (يطرد الزيوت). نظرًا لأنه يطرد كل شيء تقريبًا، فلا يوجد "مقبض" كيميائي يمكن للجزيئات الأخرى التشبث به، وهو ما يمثل الخطوة الأولى المطلوبة للهجوم الكيميائي.
الآثار العملية للمقاومة الكيميائية
تترجم هذه الاستقرار الجزيئي مباشرة إلى أداء موثوق به في البيئات الصناعية والمختبرية القاسية.
ثابت في البيئات المسببة للتآكل
نظرًا لصعوبة كسر روابطه، فإن التفلون خامل تجاه الغالبية العظمى من المواد الكيميائية المسببة للتآكل، بما في ذلك الأحماض القوية والقواعد القوية العدوانية.
يبقى مستقرًا عبر نطاق واسع جدًا من الأس الهيدروجيني (pH) حيث تتحلل العديد من المواد الأخرى بسرعة، بما في ذلك المعادن عالية الجودة.
مقاومة المذيبات والاختراق الكيميائي
تجعل نفس المبادئ التفلون مقاومًا للغاية للمذيبات العضوية. يمنع التركيب الجزيئي الكثيف والسطح غير القطبي المذيبات من إذابة المادة أو تورمها أو تسربها ماديًا إليها.
يضمن هذا الحفاظ على السلامة الهيكلية ونقاء مكون التفلون حتى مع التعرض الكيميائي المطول.
فهم المفاضلات والقيود
على الرغم من أن مقاومته الكيميائية عالمية المستوى، إلا أن التفلون ليس حلاً لا يُقهر لكل مشكلة هندسية. يتطلب الموضوعية الاعتراف بقيوده.
الضعف أمام عوامل محددة
على الرغم من خموله، يمكن مهاجمة التفلون بواسطة عدد قليل من المواد شديدة التفاعل. وتشمل هذه المعادن القلوية المنصهرة (مثل الصوديوم)، والعوامل المفلورة القوية. هذه استثناءات متخصصة ولكن من الضروري معرفتها للتطبيقات المتخصصة.
التحلل الحراري
للتفلون حد خدمة لدرجة الحرارة محدد، عادة حوالي 260 درجة مئوية (500 درجة فهرنهايت). فوق هذه الدرجة، يمكن أن تبدأ روابط C-F في التفكك، مما لا يعرض المادة للخطر فحسب، بل يمكن أن يطلق أيضًا أبخرة سامة.
القوة المادية مقابل القوة الكيميائية
من الضروري التمييز بين المقاومة الكيميائية والقوة الميكانيكية. التفلون مادة ناعمة نسبيًا ذات مقاومة ضعيفة للتآكل والخدش و"الزحف" (التشوه تحت الحمل). خموله الكيميائي لا يعني أنه قوي ميكانيكيًا.
اتخاذ الخيار الصحيح لتطبيقك
يتطلب اختيار المادة المناسبة مواءمة خصائصها الأساسية مع تحديك الأساسي.
- إذا كان تركيزك الأساسي هو احتواء الأحماض أو القواعد أو المذيبات العدوانية: يعتبر التفلون خيارًا أول استثنائيًا بسبب الاستقرار الذي لا مثيل له لرابطة الكربون والفلور.
- إذا كان تطبيقك يتضمن إجهادًا ميكانيكيًا عاليًا أو تآكلًا: يجب أن تدرك أن الخمول الكيميائي للتفلون لا يترجم إلى متانة مادية، وقد تكون هناك حاجة إلى درجة مقواة أو مادة مختلفة.
- إذا كنت تعمل بالقرب من 260 درجة مئوية (500 درجة فهرنهايت) أو أعلى: يجب أن تأخذ في الاعتبار نقطة التحلل الحراري للتفلون وتختار مادة ذات درجة حرارة أعلى إذا لزم الأمر.
يعد فهم البنية الجزيئية البسيطة والقوية للتفلون هو المفتاح للاستفادة الصحيحة من مقاومته الكيميائية المذهلة في مشروعك.
جدول الملخص:
| الخاصية | الفائدة للمقاومة الكيميائية |
|---|---|
| روابط C-F قوية | يوفر بنية جزيئية مستقرة وغير تفاعلية. |
| غلاف الفلور | يخلق حاجزًا لا يمكن اختراقه ضد العوامل المسببة للتآكل. |
| طاقة سطح منخفضة | يطرد الماء والزيوت والمذيبات، مما يمنع الهجوم الكيميائي. |
| مقاومة واسعة للأس الهيدروجيني | يبقى خاملًا لمعظم الأحماض والقواعد القوية. |
هل تحتاج إلى مكونات موثوقة وخاملة كيميائيًا لتطبيقك؟
في KINTEK، نحن متخصصون في تصنيع مكونات PTFE عالية الدقة مثل الحشيات والبطانات وأدوات المختبرات المخصصة. تضمن خبرتنا حماية معداتك من أقسى المواد الكيميائية في صناعات أشباه الموصلات والطب والمختبرات والصناعات.
دعنا نقدم لك الحل المتين والمقاوم للتآكل الذي تحتاجه.
اتصل بخبرائنا اليوم للحصول على عرض أسعار مخصص!
دليل مرئي
المنتجات ذات الصلة
- مفاعل بوليتري فلورو إيثيلين (PTFE) قابل للتخصيص وقارورة تفلون مقاومة للتآكل
- كرات تفلون PTFE مخصصة للتطبيقات الصناعية المتقدمة
- زجاجة تفاعل المذيبات المخصصة من بولي تترا فلورو إيثيلين (PTFE) بفوهة عريضة مقاومة للتآكل ودرجات الحرارة العالية بسعة كبيرة وجسم مستقيم لأوعية المختبرات
- قارورة تفاعل صغيرة من بتفف مقاومة للتآكل خزان إذابة عينات من التفلون مكون من قطعة واحدة حاوية تخزين من البوليمر الفلوري
- حقنة PTFE سعة 50 مل مقاومة للمواد الكيميائية ودرجات الحرارة العالية، محقن تفلون مخصص بخيط مانع للتسرب للتحليل النزري
يسأل الناس أيضًا
- ما هي الخصائص الرئيسية لمادة PTFE التي تجعلها قيّمة؟ افتح الأداء الفائق للبيئات القاسية
- ما هي عيوب PTFE/التفلون؟ فهم حدوده الميكانيكية وحدود التصنيع الخاصة به
- ما هي الخصائص الرئيسية التي تجعل التفلون قابلاً للتطبيق على نطاق واسع؟ اكتشف مقاومة كيميائية وحرارية لا مثيل لها
- ما هو معامل الاحتكاك للتفلون النقي؟ افتح أداء فائقًا للاحتكاك المنخفض
- ما هي المزايا الإجرائية لتشغيل مادة التفلون آلياً؟ إنتاج عالي السرعة مع استقرار حراري فائق